2024年4月5日までに、小林製薬から報告を受けていた「紅麹を含む食品に係る自主点検」の結果について、点検対象の製造業者の製品に係る自主回収届出を受理した地方自治体から厚生労働省に照会があり、厚生労働省から小林製薬に確認を求めたところ、同社からの報告に係る不備があったことが判明しました。
この自主点検に当たっては、厚生労働省から小林製薬に対し、報告対象の基準として、以下の2つを示していました。
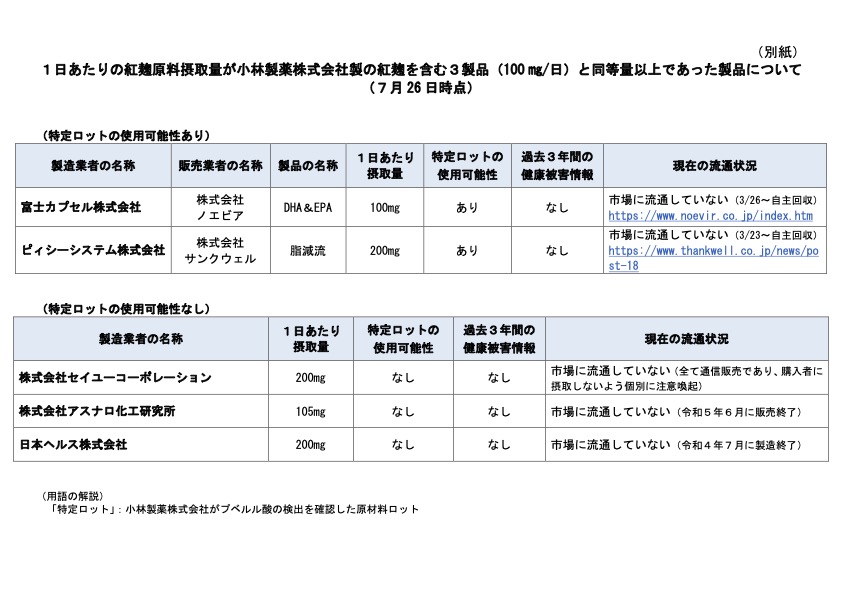
- 小林製薬の3製品に使用された紅麹と同じ小林製薬社製の原材料を用いて製造され、かつ、上記3製品と同等量100mg/1製品)以上の紅麹を1日あたりに摂取する製品
- 過去3年間で医師からの当該製品による健康被害が1件以上報告された製品
小林製薬からは、報告に係る不備事案として、製造のみで販売を行っていない社(5社)を厚生労働省への報告対象から除外していたとの報告がありました。
厚生労働省は、小林製薬からの報告を受けて、直ちに地方自治体と協力し、小林製薬から示された5社に関する安全情報(紅麹1日あたり摂取量、特定ロットの使用可能性、現在の流通状況)に関する調査を実施しており、その内容については、別紙のとおりとなっています。
小林製薬に対しては、自主点検の結果について早急に再確認し、遅くとも7月31日までに結果を報告するよう指示しています。
なお、特定ロットの使用可能性がある2製品については、各社において服用の中止を要請するとともに、自主回収が行われています。